美國
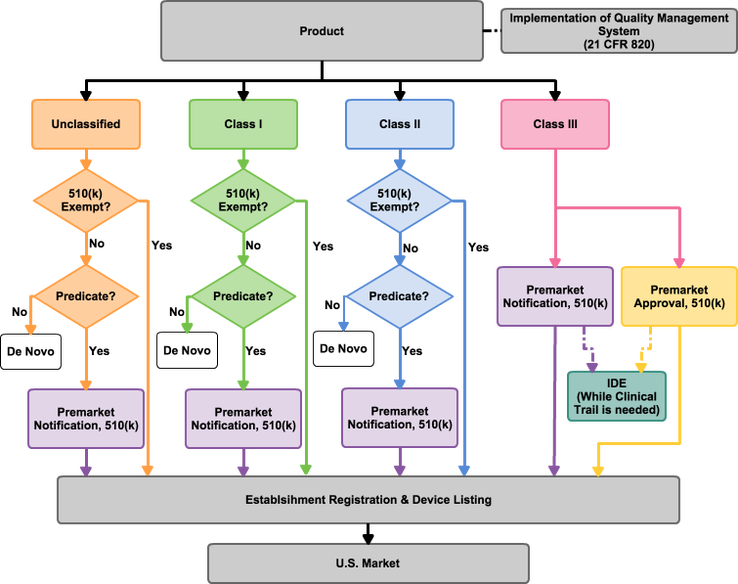
對要進入美國市場的醫療器材,產品必須要依據美國食品藥品監督管理局(FDA)的規範進行分類,分類成無分級(Unclassified)、第一級、第二級、第三級。每一級別的醫療器材可以歸類到對應的產品分類編號並藉此了解所需遵循的法規。要在美國進行醫療器材販售,廠商需要取得許可或核准。大多數的第二級醫療器材需要通過上市前通知 510(k),而第三級的醫療器材則是依照產品分類編號來決定需要申請上市前通知510(k)還是要申請上市前核准(PMA)。正常來說只有少數510(k)以及多數PMA在申請過程中會需要用到臨床報告佐證產品的安全和有效。要進行臨床試驗,實驗的步驟和手續要經過臨床試驗計畫書申請(IDE)來核查後才能進行。一旦提交充足的資料報告並通過美國食品藥品監督管理局的審查後,美國食品藥品監督管理局會給予上市許可或核准。
510(k)是上市前所需進行的FDA申請,為的是向美國食藥局證明器材在安全性和有效性上與現在合法市場上販售的器材是實質相等的。由於510(k)是基於實質相等性來申請的,尋找相似的醫療器材是非常重要的。相對來說上市前許可的模式則是著重於醫療器材本身的安全性以及有效性。不同的申請方法要求申請人提出不同文件,弘亞能夠協助我們的客戶以效率並且經濟的方式來準備資料、撰寫報告。取得上市許可或核准後,廠商可以進行公司註冊和產品列名。如果是免除510(k)和PMA的第一級醫療器材則是只要完成公司註冊和產品列名即可上市販賣。依據美國食品藥品監督管理局規定,國外廠商需要指定一個美國代理人作為美國食品藥品監督管理局和廠商間聯絡的窗口。
弘亞生技顧問有限公司有著多年協助客戶進入美國市場的法規諮詢和品質系統輔導經驗,我們輔導客戶準備並申請公司註冊、產品列名、上市前通知510(k)、上市前核准(PMA)、以及臨床試驗計畫書申請。歡迎聯絡我們任何關於進入美國醫療器材市場的問題。
510(k)是上市前所需進行的FDA申請,為的是向美國食藥局證明器材在安全性和有效性上與現在合法市場上販售的器材是實質相等的。由於510(k)是基於實質相等性來申請的,尋找相似的醫療器材是非常重要的。相對來說上市前許可的模式則是著重於醫療器材本身的安全性以及有效性。不同的申請方法要求申請人提出不同文件,弘亞能夠協助我們的客戶以效率並且經濟的方式來準備資料、撰寫報告。取得上市許可或核准後,廠商可以進行公司註冊和產品列名。如果是免除510(k)和PMA的第一級醫療器材則是只要完成公司註冊和產品列名即可上市販賣。依據美國食品藥品監督管理局規定,國外廠商需要指定一個美國代理人作為美國食品藥品監督管理局和廠商間聯絡的窗口。
弘亞生技顧問有限公司有著多年協助客戶進入美國市場的法規諮詢和品質系統輔導經驗,我們輔導客戶準備並申請公司註冊、產品列名、上市前通知510(k)、上市前核准(PMA)、以及臨床試驗計畫書申請。歡迎聯絡我們任何關於進入美國醫療器材市場的問題。