台灣
無論台灣或海外公司要在台灣進行醫療器材與體外試劑販賣,都需要符合台灣衛生福利部食品藥物管理署的先關法規規範,食藥署基於危險等級將醫材分類為第一級、第二級以及第三級。台灣的分級規範類似於美國的分級系統,第一級為低分險之器材,第二級與第三級則是有較高風險,而不論是哪一等級在上市前皆須通過食藥署的許可。
要取得上市許可,國外的醫療廠商需要指定一個在台灣本地的代表,來管理並進行產品註冊過程並作為海外廠商和食藥署的聯絡窗口。台灣代表需要有在台地址並且持有正式的藥商許可執照,也負責在提交申請上市許可所需之檔案。於申請的過程中,醫療器材廠商需要有品質系統文件(QSD)來證明製造過程符合美國的品質系統規範(QSR) 或是ISO 134850:2003。根據我們之前的經驗,衛服部食藥署較偏好ISO 13485:2003。一但經確認品質系統符合規範,食藥署會給予國外廠商輸入醫療器材品質系統文件(QSD)認可,此認可三年內有效。此外外國醫療器材廠商需要取得外國政府認證(CFG)來證明此器材先前已在海外販售。QSD與CFG都是外國廠商申請上市許可所需的必備文件。至於國內廠商不須這兩份文件,但必須取得優良製造規範(GMP)以進行上市許可申請。
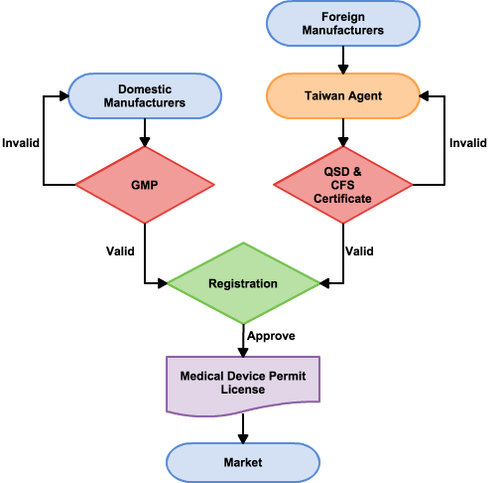
在取得這些認證文件後,就可以向食藥署提出充足的資料來進行產品登記。廠商應該提交產品資訊、產品測試報告、臨床報告(假如有需求)、以及其他產品相關文件。在國外進行之檢測通常被食藥署承認。在通過食藥署的審核後,廠商可以取得醫療器材販賣許可執照,可以開始進行販售。醫療器材販賣許可執照有效期為五年,如要更新請於過期前六個月提除申請,下面的流程圖為簡約的申請流程。弘亞生技幫助客戶申請GMP、QSD、CFS、以及註冊流程。
要取得上市許可,國外的醫療廠商需要指定一個在台灣本地的代表,來管理並進行產品註冊過程並作為海外廠商和食藥署的聯絡窗口。台灣代表需要有在台地址並且持有正式的藥商許可執照,也負責在提交申請上市許可所需之檔案。於申請的過程中,醫療器材廠商需要有品質系統文件(QSD)來證明製造過程符合美國的品質系統規範(QSR) 或是ISO 134850:2003。根據我們之前的經驗,衛服部食藥署較偏好ISO 13485:2003。一但經確認品質系統符合規範,食藥署會給予國外廠商輸入醫療器材品質系統文件(QSD)認可,此認可三年內有效。此外外國醫療器材廠商需要取得外國政府認證(CFG)來證明此器材先前已在海外販售。QSD與CFG都是外國廠商申請上市許可所需的必備文件。至於國內廠商不須這兩份文件,但必須取得優良製造規範(GMP)以進行上市許可申請。
在取得這些認證文件後,就可以向食藥署提出充足的資料來進行產品登記。廠商應該提交產品資訊、產品測試報告、臨床報告(假如有需求)、以及其他產品相關文件。在國外進行之檢測通常被食藥署承認。在通過食藥署的審核後,廠商可以取得醫療器材販賣許可執照,可以開始進行販售。醫療器材販賣許可執照有效期為五年,如要更新請於過期前六個月提除申請,下面的流程圖為簡約的申請流程。弘亞生技幫助客戶申請GMP、QSD、CFS、以及註冊流程。